今天给大家介绍的文章通过孟德尔随机化(Mendelian randomization, MR)分析结合表达量性状位点(expression quantitative trait loci, eQTL)的助力,更精准地定位了药物作用的靶点,研究者不仅识别了潜在的药物靶标,还通过药物再利用策略发现了现有药物的新适应症,文章是由四川大学华西医院陈永平课题组联合华西基法学院王祎课题组共同造就。MR是一种巧妙地利用自然发生的遗传变异作为探究因果关系的工具。而eQTL则相当于一张精细的基因调控地图,它揭示了基因变异如何调控基因表达的奥秘。这张地图已经成为全球范围内关联研究(genome-wide association studies, GWAS)的得力助手,指引着研究人员在药物靶点发现的旅途上,探索多种复杂疾病的深层次机制(是不是看到这里觉得好复杂,有种望而却步的感觉?没关系哦,小谷可以帮你快速克服困难,助力你快速发表高质量文章哦!)。小云就给你介绍这篇文章的精妙之处!
1、文章使用了来自eQTLGen和PsychENCODE血液和大脑组织的3万+个eQTLs数据,大大增加了研究结果的可靠程度;
2、研究使用MR分析,减少混杂因素的影响,提高了因果推断的准确性。
3、文章中的药理学验证实验增强了MR分析结果的可信度,特别是在细胞模型中对R788和AMX两种药物的疗效进行了验证。
这篇文章精妙地结合孟德尔随机化分析与药物再利用策略,开辟了一条高效且创新的研究路径。有了这样的思路,何愁发不了高分文章呢。你是不是也想要发表自己的优秀论文,如果你有任何想法都可以主动来找小云交流哦,如果暂时没有想法也没有关系,现在扫码添加小云微信,手把手带你发表高分论文哦!
定制生信分析
云服务器租赁
(加微信备注99领取试用)
题目:TBK1,肌萎缩侧索硬化症的优先药物再利用靶点:来自可成药基因组孟德尔随机化和体外药理学验证的证据
肌萎缩侧索硬化症(ALS)是一种致命的运动神经元疾病,目前缺乏有效的治疗策略。由于ALS的发病机制尚不完全清楚,导致治疗手段的发展面临重大挑战。因此,药物再利用,即发现现有药物的新适应症,为ALS治疗提供了一种快速且成本效益高的潜在途径。
|
|
|
|
|
|
|
|
|
|
|
679名健康对照样本;497 名精神分裂症患者、172 名双相情感障碍患者、31 名自闭症谱系障碍患者、 8 名情感障碍患者
|
首先通过MR分析和共定位分析,结合药物基因组和ALS的GWAS数据,筛选出与ALS显著相关的潜在药物靶标基因。然后,研究者根据这些基因进行药物再利用的探索,筛选出有潜力的老药新用药物候选。最后,通过细胞模型进行药效学验证,评估这些候选药物对ALS治疗的潜在效果,特别是针对TBK1、TNFSF12和GPX3这些基因的药物,以期为ALS患者找到有效的治疗手段。
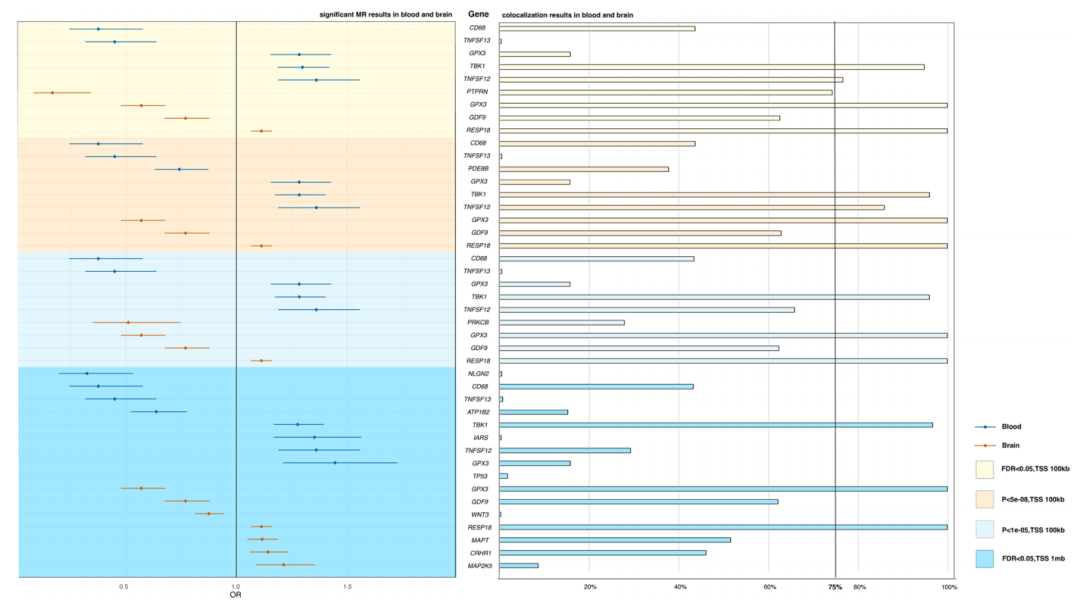
研究者使用位于TSS±100kb内且满足FDR<0.05的SNPs的显著阈值,在血液和脑中发现了8个独特的潜在药物靶点(TNFSF13、CD68、TNFSF12、TBK1、RESP18、GDF9、PTPRN和GPX3)。通过MR分析识别出与ALS风险显著相关的基因,比如在血液中TNFSF13和CD68与ALS风险降低相关;在大脑中,RESP18的表达与ALS的风险相关。共定位分析的条形图则进一步验证了MR分析中得到的显著基因与ALS的GWAS信号的共定位关系(图1)。
2、AMX和R788作为靶向TBK1的潜在抑制剂的鉴定
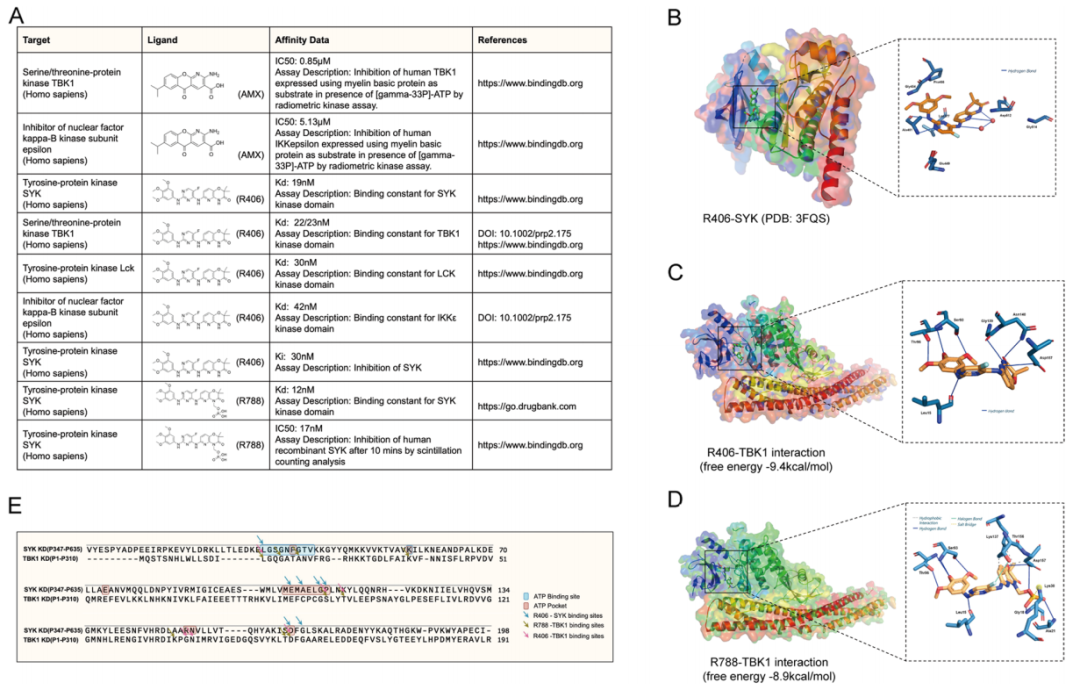
研究者采用细胞热转移实验(CETSA),发现AMX对细胞裂解物中TBK1热稳定性的影响在37-60℃的温度范围内表现出适度的差异。通过在线数据库LINCS、DrugBank和BindingDB,研究者发现R406与TBK1具有很强的亲和力(图2A)。已发表的共晶体结构表明,R406嵌入了SYK激酶结构域,并占据了ATP结合口袋(图2B);且R788和R406都很好地适合于Tbk1激活区(图2C,D)。预测的R788-TBK1相互作用表现为氢键、疏水相互作用、卤素键和盐桥(图2E)。
图2 AMX和R788作为靶向TBK1的潜在抑制剂的鉴定
3、R788和AMX抑制MSA-2诱导的cGAS/STING活性
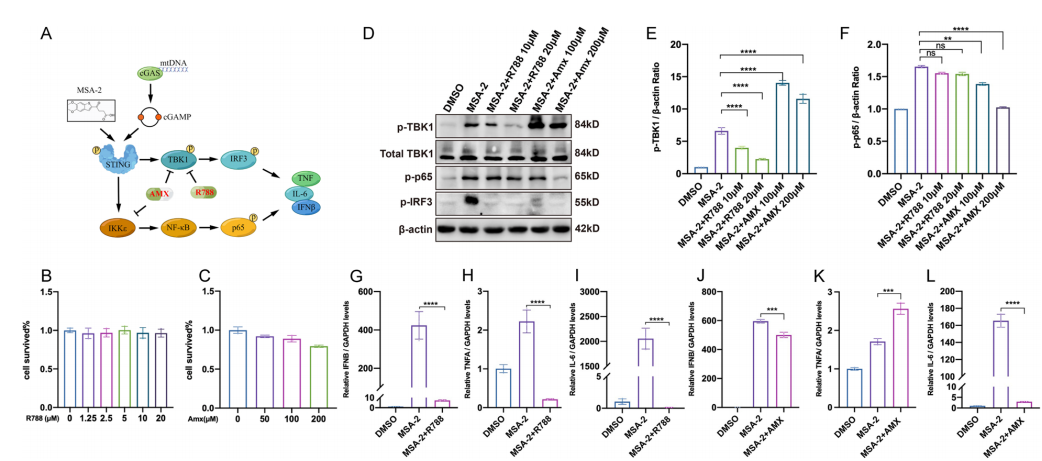
MSA-2通过Tbk1/irf3轴和IKKε/NF-ҡB轴激活cGAS/STING通路(图3A)。研究者发现R788或AMX对CCK-8的细胞毒作用呈浓度依赖关系(图3B,C)WB结果显示,R788对TBK1/IRF3信号通路中的TBK1具有特异性抑制作用。而AMX降低了p-p65和p-IRF3的水平,同时进一步增强了TBK1的磷酸化(图3D-F)。研究者还发现R788可以有效地抑制IFNB、TNFA和IL-6的诱导,AMX有效降低了IFNB和IL-6水平(图3G-L)。
图3 R788和AMX抑制MSA-2诱导的cGAS/STING活性
4、R788和AMX抑制ALS相关毒性蛋白介导的cGAS/STING信号转导
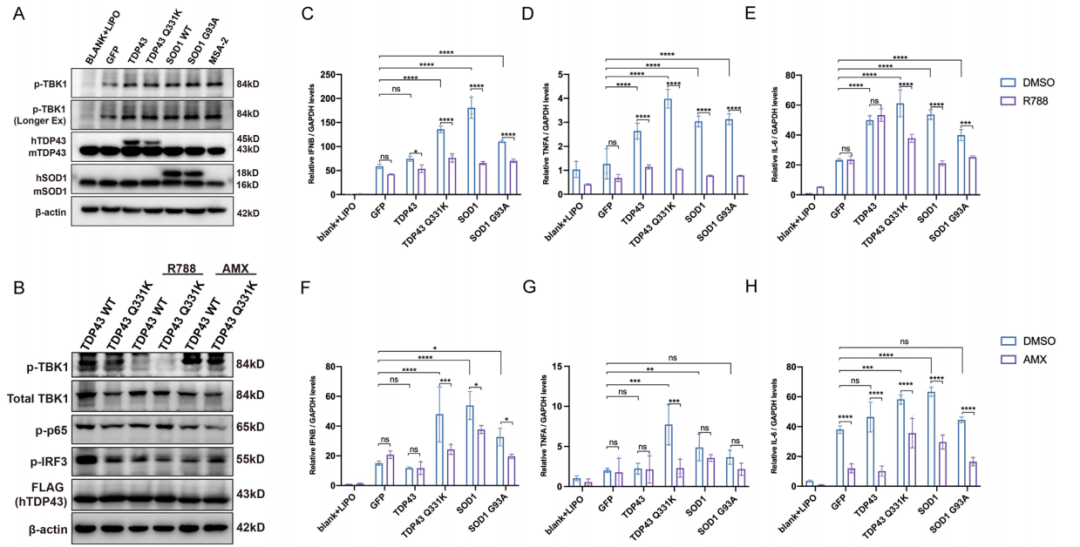
研究者通过WB观察到,转染TDP-43和SOD1相关质粒的组别中p-TBK1的水平有所增加(图4A);应用强力霉素诱导系统在NSC-34细胞中表达TDP43和Q331K突变质粒后,p-TBK1和p-IRF3被R788显著抑制(图4B)。RT-qPCR数据显示,R788和AMX抑制了在过度表达TDP-43 WT/Q331K或SOD1 WT/G93A的NSC-34细胞中测试的大多数下游cGAS/STING效应物的表达(图4C-F, H)。AMX对TNFA表达的明显抑制仅在TDP43 Q331K突变体中可见(图4G)。
图4 R788和AMX抑制ALS相关毒性蛋白介导的cGAS/STING信号转导
这篇文章结合MR分析和药物再利用策略,巧妙地将遗传学证据转化为潜在的ALS治疗靶点,展现了一种创新且高效的药物发现途径。这样巧妙的研究设计确实让人羡慕,羡慕的同时有没有激发起你的动力呢?大家都在进步,你可不能落后哦,现在扫码添加小云微信,快快努力,在小云的支援下,发表你的高分论文吧!
原文始发于微信公众号(云生信学生物信息学):BMC Med.|太秀!孟德尔随机化与3万+个eQTL数据碰撞出怎样精彩的火花?四川大学华西医院陈永平团队show给你看!